【背景介绍】
根据德勤《2019医药创新药汇报评估》行业报告披露,自2010年到2019年之间,全球新药回报率从10%直线下降至1.8%,但研发成本从11.9%上升至19.8%,制药领域面临“Eroom定律”困境,亟需新技术手段/方法提升新药研发成功率。
探寻药物研发失败的原因,往往在于药物在最终的人体临床试验中没有表现出足够的安全性和有效性。一般来说,候选药物在临床前通过啮齿动物和非啮齿动物模型来进行肝毒性测试,最常见的是大鼠和狗。一项覆盖150种药物导致人类不良事件的分析报告显示,大鼠和狗模型只能预测在人类身上产生71%的毒性【1】。其中由药物引发的肝损伤(Drug-induced liver injury,DILI)是最严重的,肝炎、肝细胞坏死、胆汁淤积、肝硬化和脂肪变性等临床反应,是临床药物失败的主要原因,同时引发50%以上比例的急性肝功能衰竭。另一项制药行业调查分析显示,临床前肝毒性评价对临床预测性较低,分别为33%(大鼠)、27%(狗)和50%(猴子)【2】。因而,一个新的DILI评价体系/方法作为动物实验的替代/补充用于提高临床实验成功率是至关重要的。
MIMICup灌流系统通过在体外重建三维仿生微环境,如多细胞共培养、组织-组织界面、血管灌注、液体流动等,来补充现有经典评价体系,进而辅助提升药物临床试验通过率。
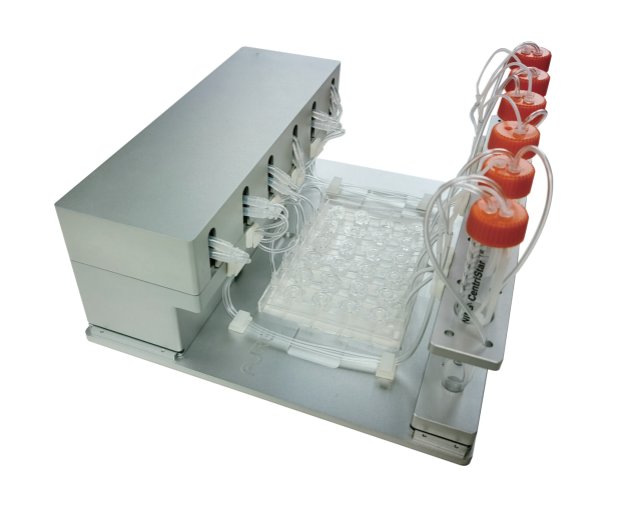
MIMICup灌流系统
【应用亮点】
可检测多种与药物诱导肝损伤(DILI)的相关的表型变化,包括肝细胞损伤、脂肪代谢异常、胆汁淤积等。
针对药物致肝毒性等不良反应的预测,将有毒性药物提前排除,提高药物研发成功率。
可兼容细胞系、类器官、组织切片多种样品并构建复杂共培养灌流培养模型
【结果】
利用细胞系在体外构建肝芯片并对芯片功能进行表征。MIMICup肝芯片由人源肝细胞与人源血管内皮细胞组成,培养小室底部为带微孔的半透膜,半透膜上侧铺有凝固的细胞外间质材料(此处为基质胶),胶表面接种肝细胞做三维培养,半透膜底部接种有贴壁生长的血管内皮细胞,培养小室底部与流道结构形成密封的微流道腔室,此腔室可进行连续的培养基灌流,构建内皮细胞所需的剪切力微环境。如下图一所示,MIMICup培养小室上下可形成底部动态灌流的细胞培养体系。
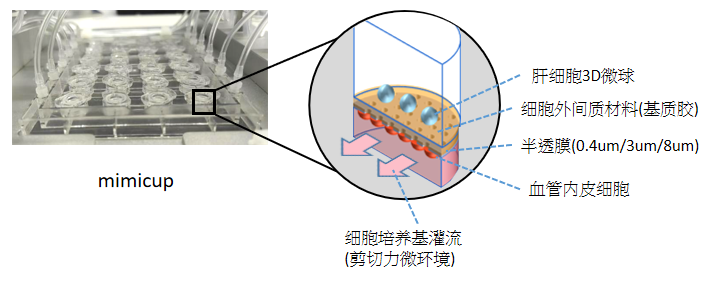
图一、MIMICup肝芯片结构图
如图二所示,针对经过14动态灌流培养的MIMICup肝芯片进行与之对应生物功能指标的检测,包含白蛋白(Albumin, ALB)、与药物代谢相关的细胞色素酶(P450)、尿素(Urea)等肝脏生理功能的表达与酶活水平检测【3】,可证明与传统2维肝细胞培养相比,MIMICup肝芯片培养体系的生理功能表达更强,在2维培养体系里无论是ALB、P450、Urea的表达均显著低于MIMICup肝芯片体系上的表达,说明MIMICup肝芯片的仿真度比起传统方法更加贴近人体生理组织。
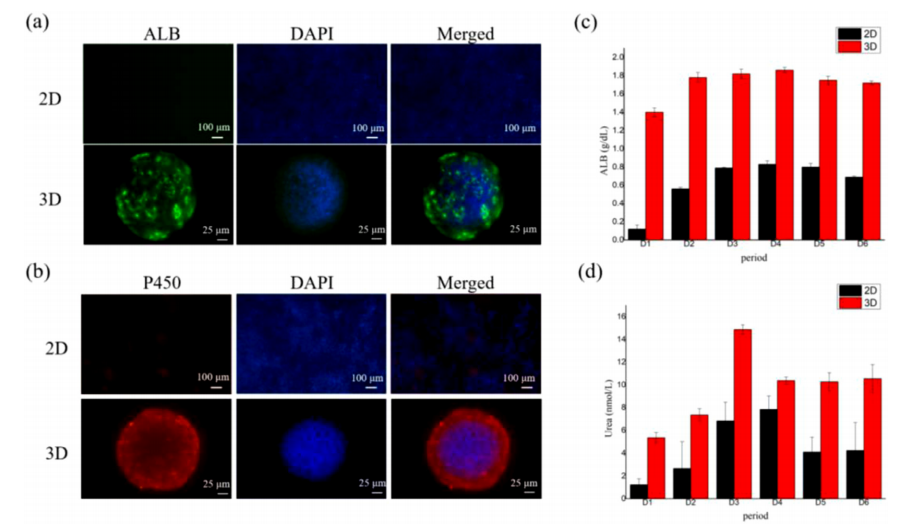
图二、MIMICup系统上构建肝芯片模型的白蛋白与P450活性表达【3】
而针对内皮细胞(HUVEC)在MIMICup肝芯片上形成的血管屏障性评估,使用原位免疫荧光染色的方式对细胞膜上表达的紧密排列蛋白与细胞骨架蛋白,包含ZO-1、VE-Cadherin、F-actin的表达强弱。由图三结果所示,与静态培养作对照可看出在动态培养构建的剪切力微环境体系的作用下,HUVEC细胞呈现与传统静态培养体系显著不同的紧密排列性质,在细胞与细胞相接触的边缘产生了ZO-1、VE-Cadherin、与F-actin的显著高表达【3】。这样的结果说明在MIMICup动态灌流培养体系的作用下,对于体外培养人体组织中由细胞组成的屏障结构有促进生成的效果,可用于体外血管屏障模型的构建,利于提升带有屏障性质的细胞在体外表现出高度紧密连接的生长状态。
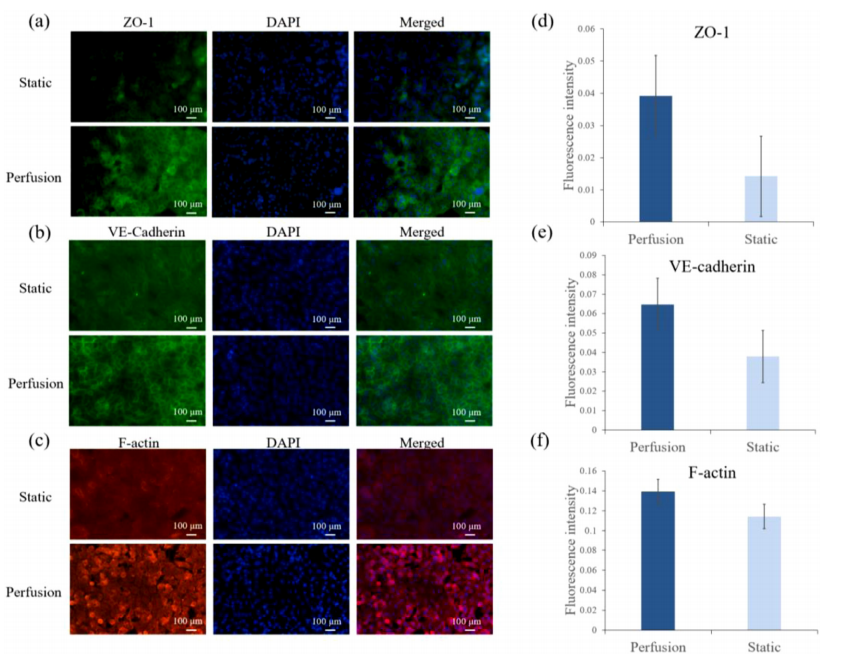
图三、MIMICup系统上HUVEC细胞的屏障性检测【3】
曲格列酮(Troglitazone)为唑烷二酮类口服降血糖药物,可改善胰岛素抵抗,增加人体组织对胰岛素的敏感性,增强胰岛素的作用。但由于其不良反应显著,可见有ALT轻度可逆性增高,国外在2510例中有2例出现黄痘,且自1997年上市以来,已收到90例与曲格列酮相关的肝脏衰竭及63例死亡的报道直到2000年3月美国FDA通知撤销该品种。曲格列酮在被批准用于治疗2型糖尿病后不久,即因其肝毒性而退出市场,但在体外毒性试验、动物实验和临床试验中,均未发现其具有肝毒性,这个事实反映了现有的DILI评价体系存在的缺陷。
鉴于上述背景,为评估该芯片是否可用于评价DILI,将MIMICup肝芯片共培养体系暴露于曲格列酮中由图四可看出,随着曲格列酮的暴露浓度上升,MIMICup肝芯片中的三维培养肝细胞微球逐渐出现相应比例的细胞凋亡,并且在上清波中检测到的由肝细胞微球所分泌的白蛋白浓度也出现与之相应的表达下降,说明在曲格列酮药物暴露的条件下,MIMICup肝芯片能表现出能用评估DILI相应指标变化,相较于传统二维培养,MIMICup肝芯片显示出对于致肝毒性药物更高的灵敏度和更好的预测性能。
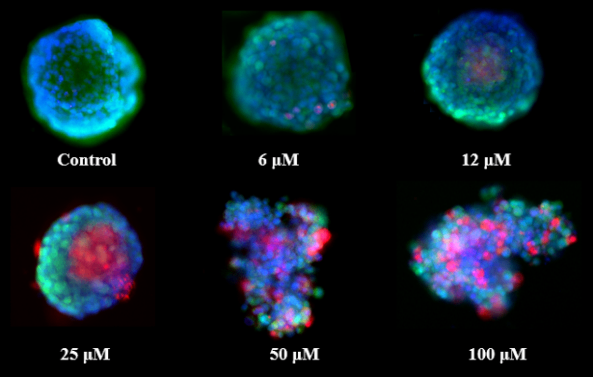
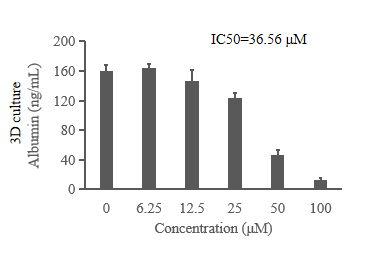
图四、MIMICup肝芯片暴露于曲格列酮药物的DILI反应
此外,为了进一步验证MIMICup肝芯片的药物肝毒性预测性能,本芯片还针对另一种临床已知会引起DILI反应的药物-对乙酰氨基酚(APAP)进行药物暴露测试【3】。由图五结果可知,在5a和5b中APAP显著诱导了肝细胞中ROS(活性氧)的产生,且这种作用表现为APAP剂量的依赖性。此外,如图5c所示,根据酶标仪测定的定量结果,4mmol/L的APAP暴露会显著降低MIMICup肝芯片的白蛋白表达量,导致这种现象的原因可由图5e推论,即经4mmoI/LAPAP处理后,肝细胞的ATP表达下降,显示细胞活力下降并出现凋亡,因此造成白蛋白的分泌表达显著下调。此结果再次验证MIMICup肝芯片在药物DILI评价方面的应用价值与潜力,有望作为一种新型的临床前药物毒性评价体系。
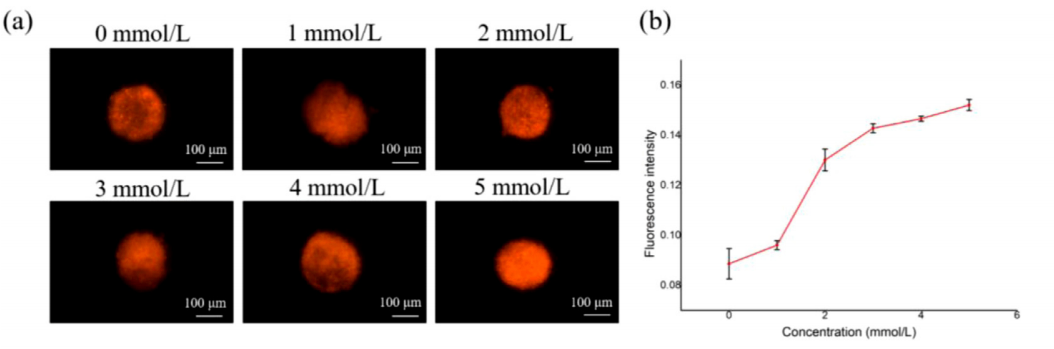
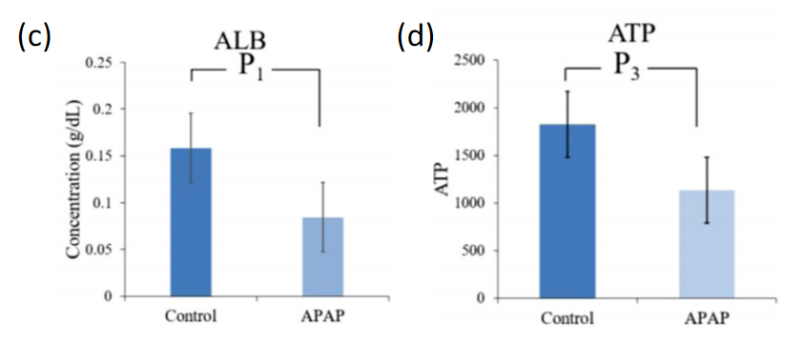
图五、MIMICup肝芯片暴露于对乙醯氨基酚的DILI反应【3】
在验证了几种已知有肝毒性的化合物药物后,我们也针对中药研究方面的应用可行性在MIMICup肝芯片上进行了评估,使用临床背景清晰的中药单体/中药注射液MIMICup肝芯片进行与上述同样的暴露实验测试结果如图六所示,实验结果显示四种在临床用药未发现明显肝毒性的注射液:包含舒血宁注射液、穿心莲注射液、清开宁注射液、香丹注射液,这些药物暴露在MIMICup肝芯片上的测试也未见显著肝毒性反应,其评估结果与药物的临床表现一致;反之,在四种临床已报导具有肝毒性的中药单体:包含吴茱萸碱、吴茱萸次碱、班鳌素、马兜铃酸A等药物的暴露实验中,MIMICup肝芯片均表现出显著的肝毒性反应,且相较于二维细胞培养这种经典法的体外模型,其肝毒性反应更为明显。
由上述结果可知,且与传统二维细胞培养经典测试法相比,MIMICup肝芯片具有更好的DILI药物识别的特异性和敏感性。
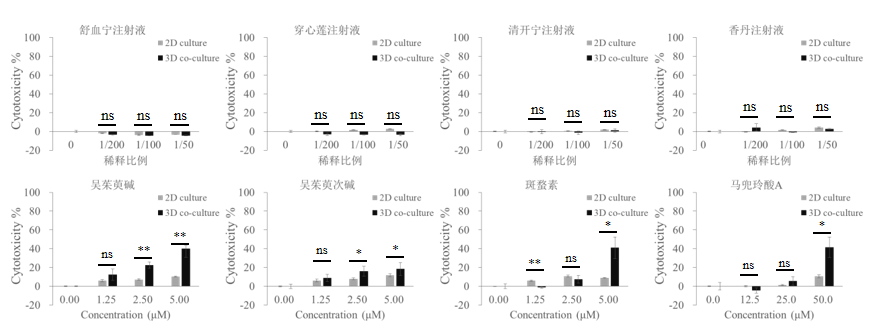
图六、MIMICup肝芯片暴露于多种中药注射液的DILI反应
除上述使用细胞接种的方式将肝细胞与内皮细胞等直接接种在MIMICup芯片上培养,从而构建可用于药物DILI评价、具备部份肝生理功能仿真特性的MIMICup肝芯片之外,使用精密肝组织切片在MIMICup体系中培养,从而构建一种新型的MIMICup肝芯片用于中药安全性评价的应用也被证明具有更好的活性和药物识别敏感性。
按常规流程将大鼠精密肝切片制备好后,将直径6mm的精密肝切片置于MIMICup培养小室内做底部带有细胞培养基连续灌流的动态培养,实验组分为与HUVEC细胞共培养与不共培养的体系,以及使用HepaRG细胞直接接种在MIMICup培养小室内的二维贴壁培养体系。药物暴露实验中分别以1.2、0.6、0.3mg生药/mL的雷公藤醇提物为循环液进行灌流,同时芯片培养小室内加入上述浓度的雷公藤醇提物的含0.5wt%,继续在37℃,5%CO2的培养箱中培养24h后,取培养上清用全自动生化分析仪对肝损伤标记物,包括谷丙转氨酶(ALT)、乳酸脱氢酶(LDH)、谷氨酰转肽酶(GGT)、甘油三酯(TG)等进行检测。
另外,取培养后的肝切片迅速置于4%甲醛溶液中固定7天后,进行脱水、透明、包埋,常规制备3um厚石蜡切片,HE染色,光学显微镜检查。结果如图七所示,在MIMICup微流控芯片体系下进行的精密肝切片培养动态培养实验组,无论在ALT、LDH、GGT、TG四个肝损伤标记物的表达上都比静态培养的肝切片体系高,即对于药物毒性反义的灵敏度也较高。
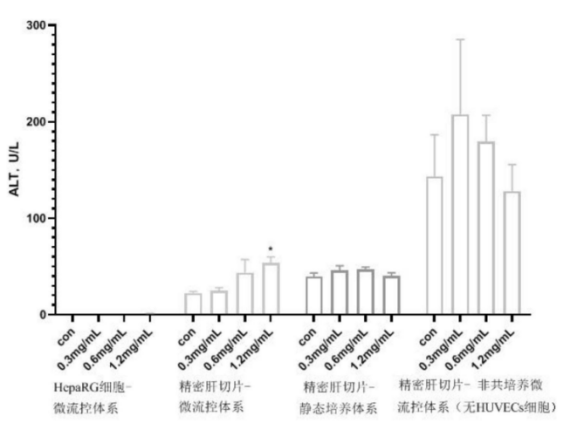
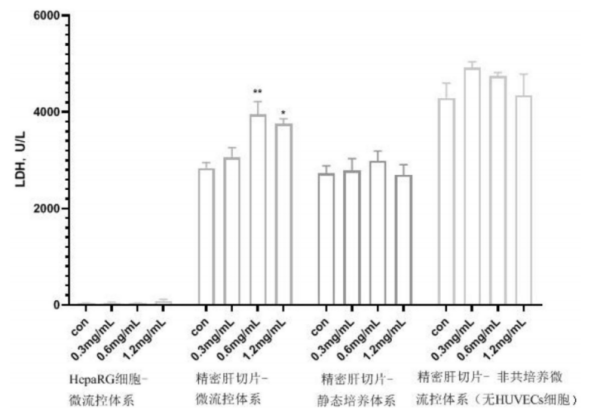
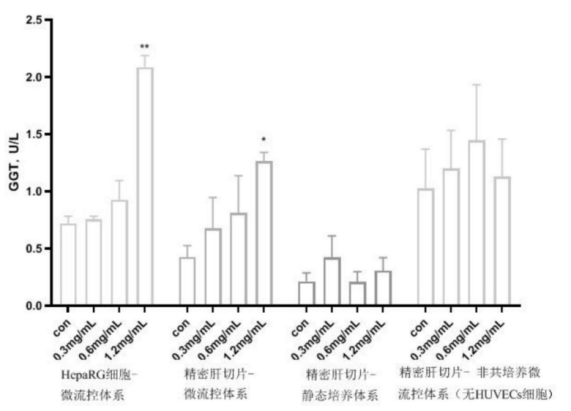
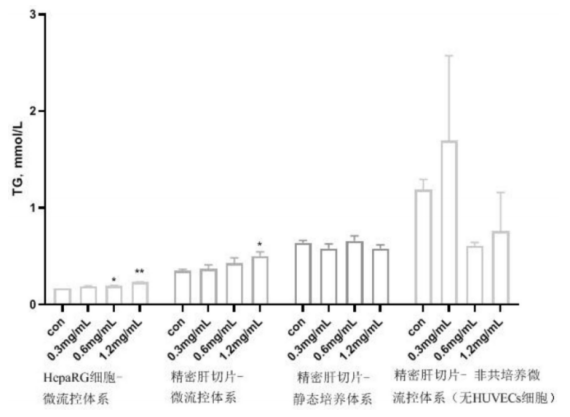
图七、MIMICup肝组织切片的药物肝毒性评估【4】
【总结】
综合上述实验结果,基于MIMICup灌流系统所搭建的肝脏芯片(或肝组织芯片)具有更好的仿生功能能够表现出比起二维细胞培养这类经典测试法更加灵敏且更具特异性的药物肝毒性反应,并得出与临床试验相似性较高的结果。由此可知,MIMICup灌流系统作为一种极具潜力的体外模型构建平台,所搭建出的肝芯片在作为药物毒性测试DILI的一种新型工具时,其表现出的优越潜力不容忽视。
【文献引用】
1. Olson, H. et al. Concordance of the toxicity of pharmaceuticals in humans and in animals. Regul. Toxicol. Pharmacol. 32, 56–67 (2000).
2. T. M. Monticello, T. W. Jones, D. M. Dambach, D. M. Potter, M. W. Bolt, M. Liu, D. A. Keller, T. K. Hart and V. J.Kadambi, Toxicol. Appl. Pharmacol., 2017, 334, 100–109.
3. Tian, T. et al. A 3D bio-printed spheroids based perfusion in vitro liver on chip for drug toxicity assays. Chinese Chemical Letters. Volume 33,Issue 6,June 2022,Pages 3167-3171.
4. 刘婷,杨依霏,夏冰,赵春晖,李春,宫平,齐莹,赵晓昂.”一种用于中药肝毒性评价的基于微流控体系的精密肝切片培养模型”,专利号:CN114854585A






